改造脂肪细胞竟能抗癌?Nat Biotechnol:CRISPRa修饰的脂肪细胞可显著抑制肿瘤发展进程 |
 |
来源:100医药网 2025-02-20 09:29
本研究利用CRISPRa技术诱导脂肪细胞褐变,通过体外、动物及临床相关实验证实,修饰的脂肪细胞和脂肪类器官能抑制多种癌细胞生长,AMT技术可靶向癌症代谢途径,展现出治疗多种癌症的潜力。
在癌症研究领域,一直以来,独特的代谢方式都是科学家们关注的焦点。肿瘤细胞如同疯狂的 掠夺者 ,为了满足自身快速增殖的需求,会想尽办法摄取和代谢大量营养物质。它们能重新编程代谢途径,即便在氧气充足的情况下,也偏好通过有氧糖酵解来获取能量,这种现象被称为 Warburg效应 。同时,在缺氧环境中,肿瘤细胞还会增加脂质的利用。
针对肿瘤细胞的这些代谢特点,科研人员尝试了多种方法来阻断其营养供应,抑制肿瘤生长。比如,研发针对糖酵解和脂质代谢关键靶点的药物,但这些方法都存在一定的局限性。就在大家不断探索新的治疗策略时,一项发表于Nat Biotechnol的研究Implantation of engineered adipocytes suppresses tumor progression in cancer models带来了新的希望 脂肪组织调控移植(AMT)技术。

AMT技术巧妙地利用了白色脂肪组织的两个特性。一方面,白色脂肪组织可以通过吸脂轻松获取,并通过手术植入体内;另一方面,它能够通过特定方式转变为类似棕色脂肪的组织,这个过程被称为 褐变 。研究人员利用CRISPRa技术,上调白色脂肪细胞中UCP1、PPARGC1A或PRDM16等基因的表达,成功诱导了脂肪细胞的褐变,使其具备更强的葡萄糖和脂肪酸摄取及代谢能力。
研究人员通过一系列实验验证了AMT技术的抗癌效果。在体外实验中,将CRISPRa修饰的脂肪细胞与多种(如、、和细胞)共培养,结果令人振奋:癌细胞的增殖明显受到抑制,葡萄糖摄取、糖酵解和脂肪酸氧化能力也显著降低。这表明,修饰后的脂肪细胞就像 营养抢夺者 ,从癌细胞手中夺走了关键营养物质,让癌细胞的生长 力不从心 。
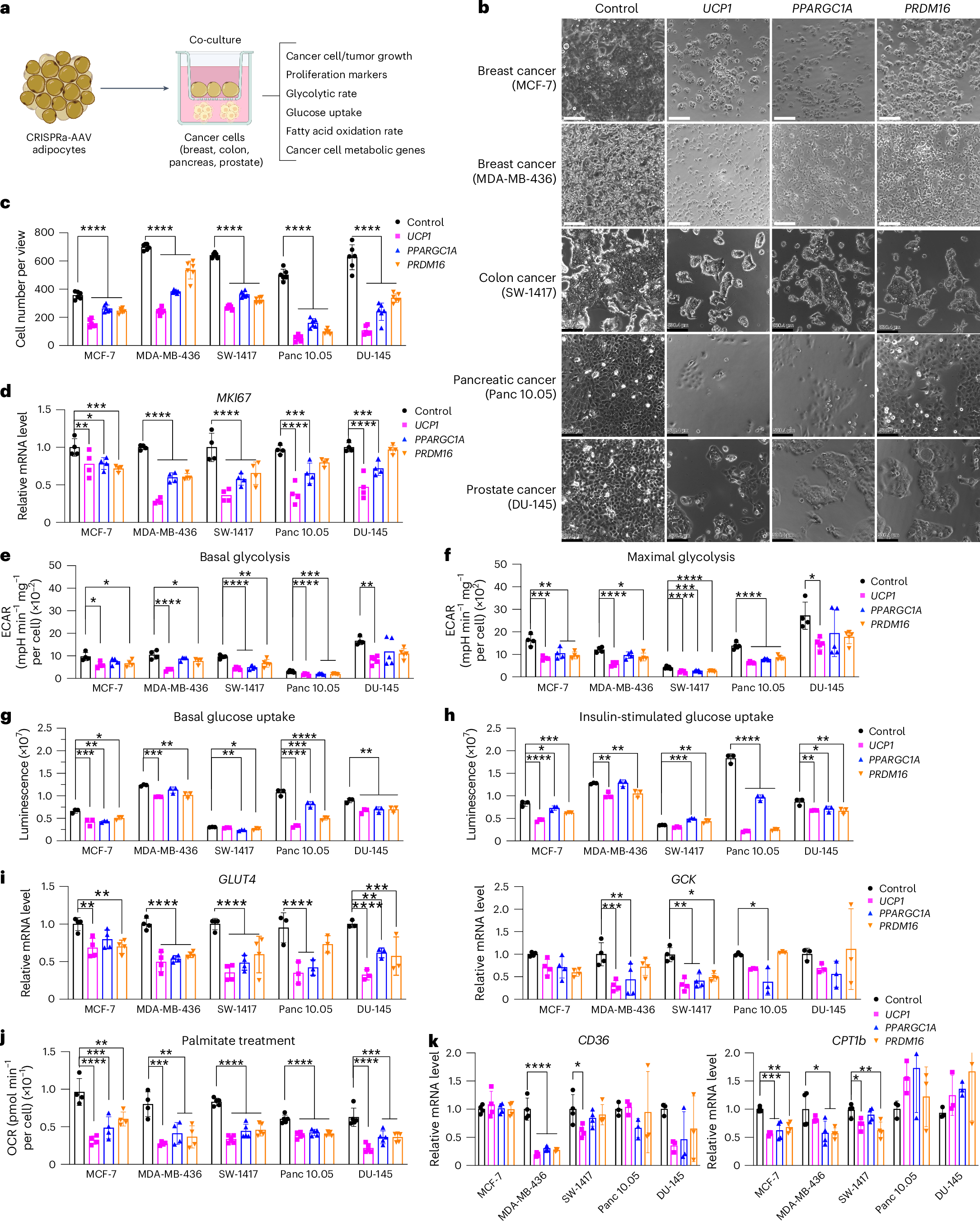
图 1:CRISPRa修饰的脂肪细胞在体外抑制癌细胞生长
在动物实验中,研究人员构建了肿瘤异种移植模型和遗传小鼠模型。在异种移植模型中,将UCP1-CRISPRa修饰的人脂肪类器官与癌细胞共移植到缺陷小鼠体内,发现肿瘤体积明显缩小,同时肿瘤的增殖、糖酵解、脂肪酸氧化相关基因表达下降,缺氧和生成情况也得到改善。在胰腺癌和乳腺癌的遗传小鼠模型中,植入UCP1-CRISPRa修饰的脂肪类器官同样有效地抑制了肿瘤的发展,降低了肿瘤代谢和增殖相关基因的表达,减少了缺氧和血管生成,还增加了癌细胞的凋亡。
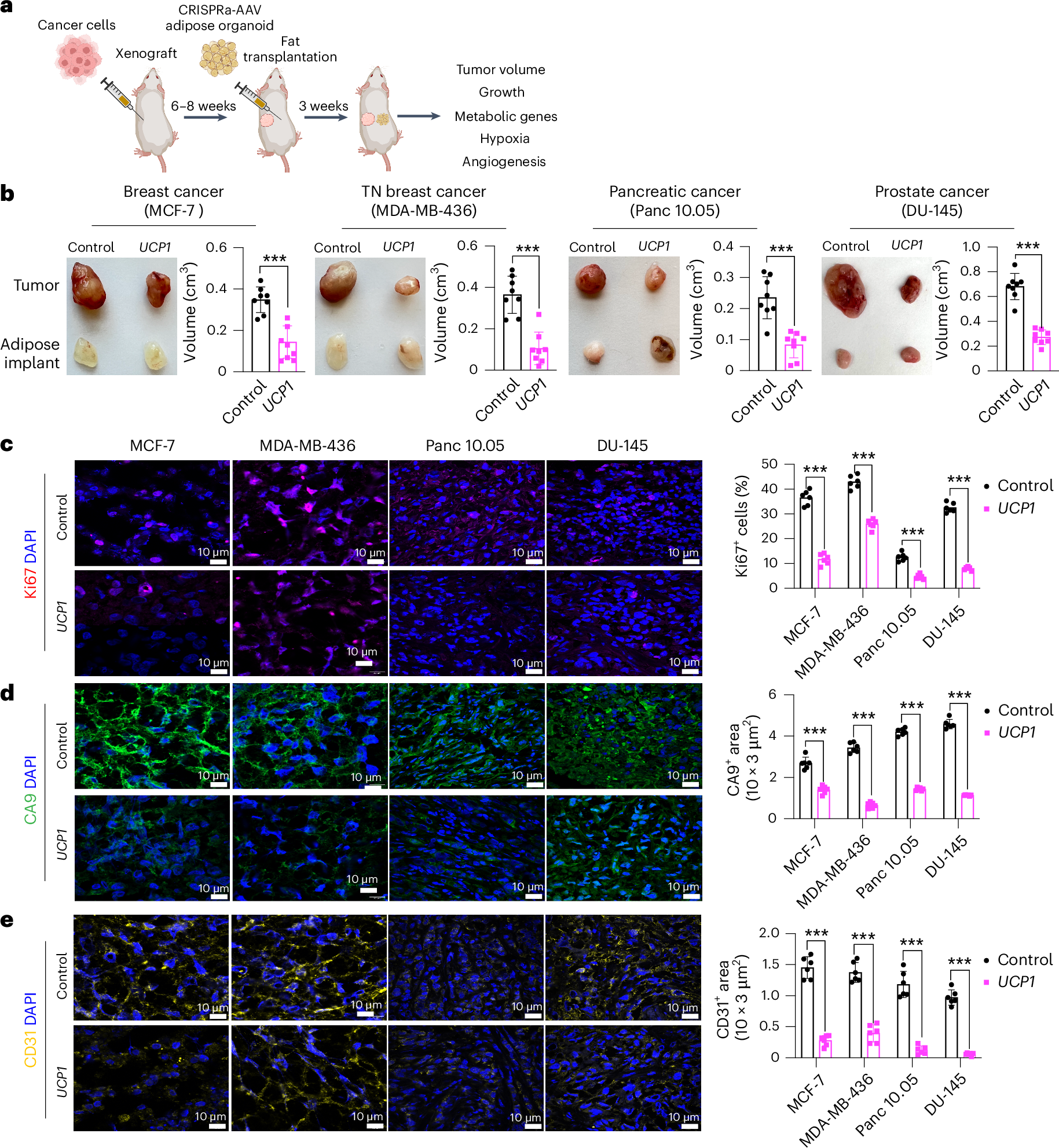
图 2:将异种移植物与UCP1-CRISPRa修饰的人脂肪类器官共移植可抑制肿瘤生长
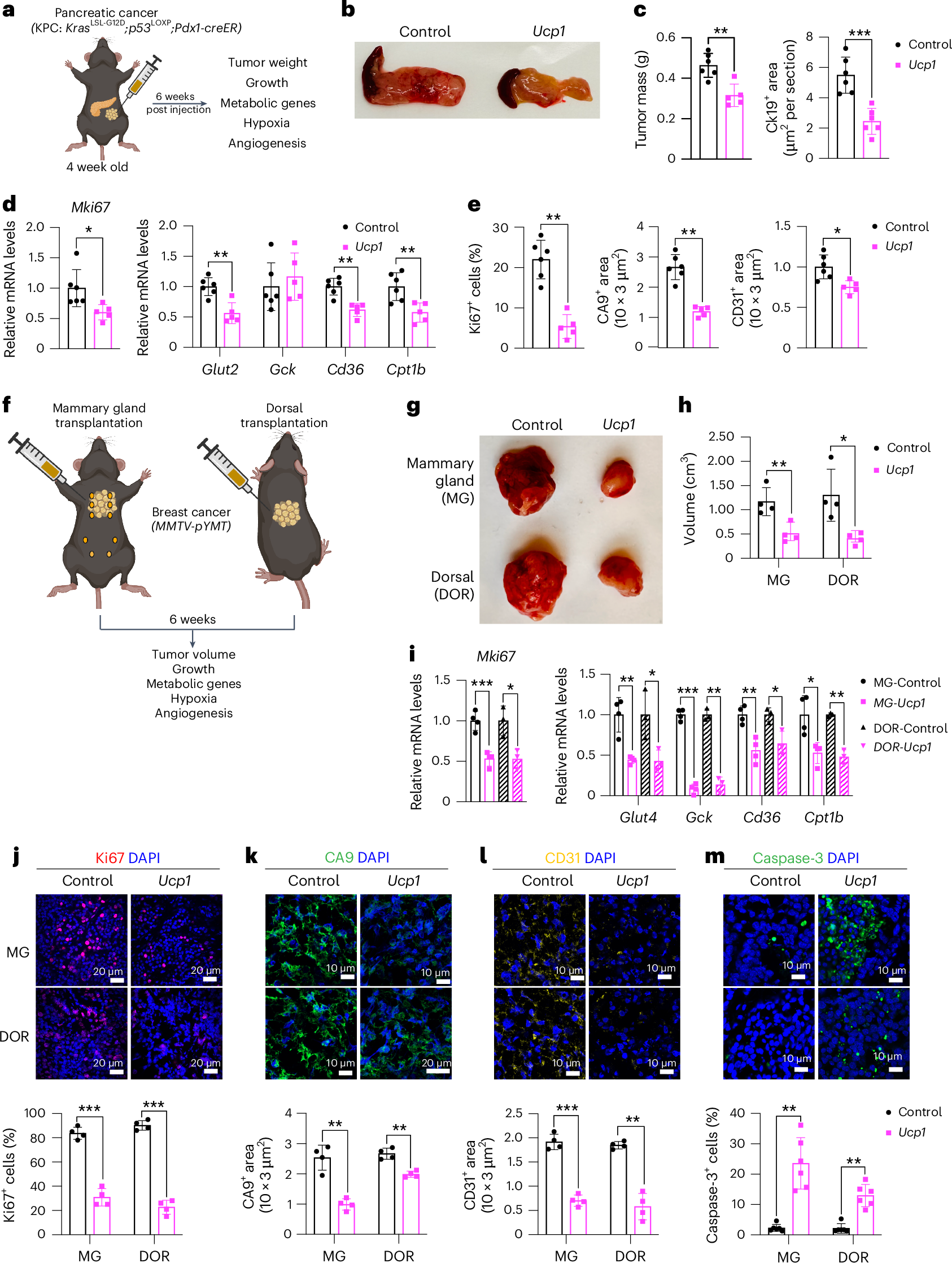
图 3:在胰腺癌和乳腺癌基因小鼠模型中植入UCP1-CRISPRa脂肪类器官可抑制癌症发展
更为重要的是,AMT技术在临床相关实验中也展现出了巨大的潜力。从人乳腺组织获取的脂肪细胞,经过UCP1-CRISPRa处理后,无论是在体外与乳腺癌类器官共培养,还是在体内植入免疫缺陷小鼠,都能显著抑制肿瘤生长。此外,AMT技术还可以通过诱导型AAV载体和细胞支架系统进行调控,进一步提高治疗的性和有效性。研究人员还发现,上调脂肪细胞中UPP1基因的表达,可以抑制依赖尿苷的胰腺导管腺癌的生长,这表明AMT技术具有针对不同癌症代谢特点进行个性化治疗的能力。
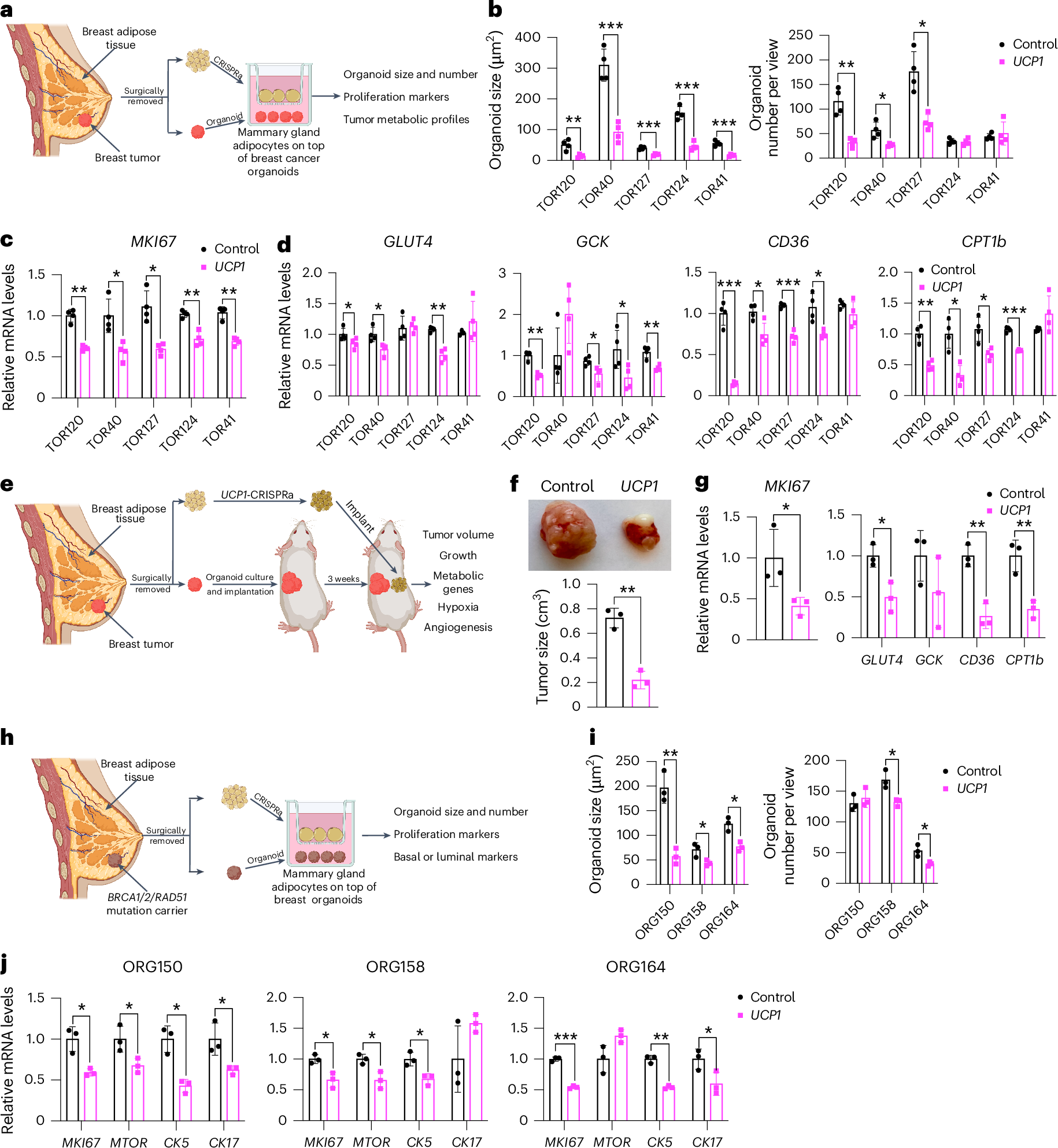
图 4:与UCP1-CRISPRa脂肪细胞(均来自解剖的乳腺组织)共培养的癌症类器官导致肿瘤抑制并预防癌症发展
总的来说,这项研究为癌症治疗开辟了一条全新的道路。AMT技术利用修饰的脂肪细胞,巧妙地靶向癌症的代谢途径,展现出了强大的肿瘤抑制能力。不过,目前该技术仍处于研究阶段,距离临床应用或许还有一段距离。但它无疑为癌症患者带来了新的希望,相信在科研人员的不懈努力下,AMT技术有望成为癌症治疗的有力武器,为攻克癌症这一难题贡献重要力量。(100yiyao.com)
参考文献:
Nguyen HP, An K, Ito Y, et al. Implantation of engineered adipocytes suppresses tumor progression in cancer models.Nat Biotechnol. Published online February 4, 2025. doi:10.1038/s41587-024-02551-2
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 《癌症通讯》:一旦感染,阴魂不散!新桥医院团队首次发现,幽门螺杆菌能将促癌“写入”宿主细胞基因组 (2025-02-24)
- 厦门大学和万泰生物联合研制生产的P85-Ab鼻咽癌诊断检测试剂盒入选2024年中国医药生物技术十大进展 (2025-02-24)
- Cell Biomaterials:北京大学林志强/张强团队全面综述脑病中的线粒体——从分子结构机制到靶向治疗 (2025-02-24)
- Cell:脑细胞模拟肌肉信号传导来增强学习和记忆 (2025-02-24)
- 柳叶刀:AAV基因疗法,帮助遗传性失明儿童重见光明 (2025-02-24)
- 血管中也有“捣蛋鬼”!Angiogenesis研究用可视化血管类器官模型,揪出“捣乱分子”,给新药研发“开绿灯”! (2025-02-24)
- Cell Stem Cell:揭示成年人类大脑中神经干细胞被激活的分子机制 (2025-02-23)
- Nature子刊:引入m7G帽结构,显著提高环状mRNA翻译效率 (2025-02-23)
- J Immunol:科学家开发出能靶向作用并杀灭HIV的新型自然杀伤性细胞策略 (2025-02-23)
- Cell:在脑干中发现阻止进食的特定神经元 (2025-02-23)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















